[버핏연구소=김인식 기자] 셀트리온(068270)이 미국소화기학회(DDW)서 ‘램시마SC 유효성 및 안전성 확인’ 글로벌 임상 3상 결과를 발표하며, FDA에 신약 허가에 대한 기대감을 모으고 있다.
셀트리온은 지난 6일부터 9일까지(현지시각) 미국 시카고 및 온라인에서 진행된 ‘2023년 미국소화기학회’에 참가해 인플릭시맙 피하주사 제형 자가면역질환 치료제 ‘CT-P13 SC (램시마SC)’의 글로벌 임상 3상 결과 2건을 각각 구두 발표 및 포스터로 공개했다.

셀트리온이 미국소화기학회에서 글로벌 임상 3상 결과를 공개하고 있다. [사진=셀트리온]
셀트리온이 이번에 공개한 연구는 크론병 환자 343명, 궤양성 대장염 환자 438명을 대상으로 진행한 글로벌 임상 3상 결과다. 셀트리온은 임상에 참여한 환자를 대상으로 6주차까지 램시마 정맥주사(IV) 제형을 투약했다. 이들 중 램시마 IV 유도요법에 임상반응을 보인 환자를 10주차에 2:1 비율로 램시마SC 투여군과 위약 대조군으로 무작위 배정하고 이후 유지 치료에서 위약 대비 램시마SC의 유효성 측면 통계적 우위 및 안전성을 확인했다.
임상 결과에 따르면, 램시마SC로 유지 치료를 받은 후 54주 시점에서 위약 대조군 대비 통계적으로 유의하게 높은 치료 유효성 결과가 도출돼 램시마SC의 우월성이 입증됐다. 안전성에서도 램시마SC 투약군이 위약 대조군과의 유의미한 차이를 보이지 않았고, 새로운 안전성 관련 우려사항도 발견되지 않았다.
해당 연구 결과는 셀트리온이 램시마SC의 미국 신약 허가를 목적으로 진행한 임상 데이터다. 램시마SC는 피하주사 제형으로 환자 편의성을 개선한 셀트리온의 차세대 전략 제품으로, 미국 식품의약국(FDA)으로부터 제품 차별성을 인정받아 신약 허가 프로세스의 진행을 권고 받았다. 이에 셀트리온은 지난해 말 FDA에 신약으로 램시마SC 허가 신청을 완료했고 올해 연말 허가 획득을 예상하고 있다.
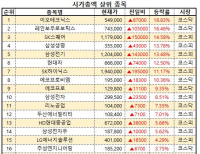
[관심 종목]
068270: 셀트리온
<저작권자 ©I.H.S 버핏연구소(buffettlab.co.kr) 무단전재 및 재배포 금지>